Detail Rangkuman Materi
Struktur Atom
Setiap materi di alam semesta ini tersusun atas partikel-partikel yang sangat kecil yang oleh para ahli dikenal dengan nama atom. Sejak dahulu kala pertama manusia berpikir tentang zat penyusun setiap materi, kemudian dirumuskannya teori atom dan sampai sekarang di zaman yang serba canggih ini, keberadaan atom sudah diterima semua orang, tetapi bagaimana bentuk sebenarnya atom tersebut serta penyusunnya belum diketahui secara pasti. Para ahli hanya mereka-reka berdasarkan pengamatan di laboratorium terhadap gejala yang ditimbulkan jika suatu materi diberi perlakukan tertentu. Dari pengamatan gejala-gejala tersebut para ahli kemudian membuat teori tentang atom dan memperkirakan bentuk atom tersebut yang dikenal dengan sebutan model atom. Model-model atom yang diusulkan oleh para ahli mengalami per-Kembangan sampai sekarang dan akan terus berkembang seiring dengan semakin canggihnya instrumen laboratorium yang ditopang oleh kemajuan iptek yang luar biasa.
Teori atom Dalton
Teori atom Dalton didasarkan atas tiga asumsi pokok, yaitu:
- Setiap unsur kimia tersusun oleh partikel-partikel kecil yang tidak dapat dihancurkan dan dipisahkan yang disebut atom. Selama mengalami perubahan kimia, atom tidak bisa diciptakan dan dimusnahkan.
- Semua atom dari suatu unsur mempunyai massa dan sifat yang sama, tetapi atomatom dari suatu unsur berbeda dengan atom-atom dari unsur yang lain, baik massa maupun sifat-sifatnya yang berlainan.
- Dalam senyawa kimiawi, atom-atom dari unsur yang berlainan melakukan ikatan dengan perbandingan angka sederhana.
Model atom Thompson
Model atom Thompson dianalogkan seperti sebuah roti kismis, di mana atom terdiri atas materi bermuatan positif dan di dalamnya tersebar elektron bagaikan kismis dalam roti kismis. Karena muatan positif dan negatif bercampur jadi satu dengan jumlah yang sama, maka secara keseluruhan atom menurut Thompson bersifat netral.
Model atom Rutherford
Model atom Rutherford menyatakan bahwa :
- Atom tersusun dari inti atom yang bermuatan positif, dan elektron-elektron bermuatan negatif yang mengelilingi inti.
- Semua proton terkumpul dalam inti atom, dan menyebabkan inti atom bermuatan positif.
- Sebagian besar volume atom merupakan ruang kosong. Hampir semua massa atom terpusat pada inti atom yang sangat kecil. Jari-jari atom sekitar 1 – 10 m, sedangkan jari-jari inti atom sekitar 10 – 15 m.
- Jumlah proton dalam inti sama dengan jumlah elektron yang mengelilingi inti, sedangkan atom bersifat netral.
Model atom Bohr
Model atom Bohr dianalogkan seperti sebuah tata surya mini. Pada tata surya, planetplanet beredar mengelilingi matahari, sedangkan pada atom, elektron - elektron yang beredar mengelilingi atom, hanya bedanya pada sistem tata surya setiap lintasan (orbit) hanya ditempati 1 planet, sedangkan pada atom setiap lintasan (kulit) dapat ditempati lebih dari 1 elektron.
Susunan ATOM
Henry Gwyn - Jeffreys Moseley (1887 – 1915) pada tahun 1913 menemukan bahwa jumlah muatan positif dalam inti atom merupakan sifat khas masing-masing unsur. Atom-atom dari unsur yang sama memiliki jumlah muatan positif yang sama. Moseley kemudian mengusulkan agar istilah nomor atom diberi lambang Z, untuk menyebutkan jumlah muatan positif dalam inti atom.
Nomor atom unsur menunjukkan jumlah proton dalam inti. Setelah dilakukan percobaan, diketahui bahwa atom tidak bermuatan listrik yang berarti dalam atom jumlah muatan positif sama dengan jumlah muatan negatif, sehingga nomor atom juga menunjukkan jumlah elektron dalam unsur.
| Nomor Atom (Z) = | Jumlah Proton |
| = | Jumlah Elektron |
Misalnya, unsur oksigen memiliki nomor atom 8 (Z = 8), berarti dalam atom oksigen terdapat 8 proton dan 8 elektron.
Selain nomor atom, ada juga yang disebut dengan nomor massa yang biasanya diberi lambang A. Nomor massa ini digunakan untuk menentukan jumlah nukleon dalam atom suatu unsur. Nukleon sendiri adalah partikel penyusun inti atom yang terdiri dari proton dan neutron.
A = P + N
Keterangan :
A = Nomor Massa
P = Jumlah Proton
N = Jumlah Neutron
Dalam penulisan atom, nomor massa (A) ditulis di sebelah kiri atas, sedangkan nomor atom (Z) ditulis di sebelah kiri bawah dari lambang unsur.
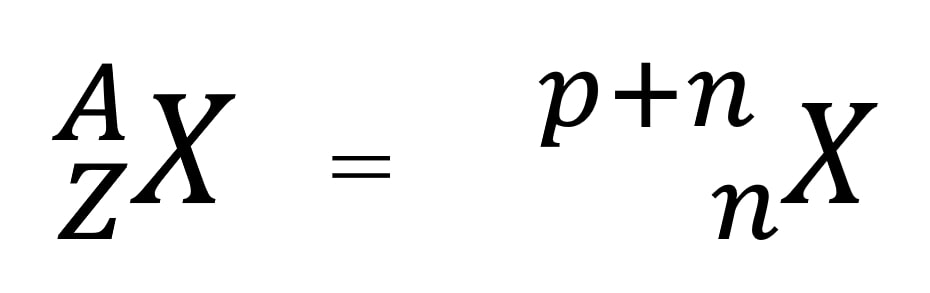
Keterangan :
X = Lambang Unsur
A = Nomor Massa
Z = Nomor Atom
Untuk ion (atom bermuatan positif atau negatif) maka notasi ion, jumlah proton, neutron, dan elektron adalah :

Untuk atom netral, jumlah proton sama dengan jumlah electron.
- - Untuk ion positif, jumlah proton atau muatan positif lebih banyak daripada elektron atau muatan negatif.
- - Untuk ion negatif, jumlah elektron atau muatan negatif lebih banyak daripada jumlah proton atau muatan positif.
Isotop, Isobar dan Isoton
- - Isotop adalah atom dari unsur yang sama, tetapi berbeda massa. Perbedaan massa disebabkan perbedaan jumlah neutron. Atom unsur yang sama dapat mempunyai jumlah neutron yang berbeda.
- - Isobar adalah atom dari unsur yang berbeda, tetapi mempunyai nomor massa sama.
- - Isoton adalah atom dari unsur yang berbeda, tetapi mempunyai jumlah neutron sama.